Inhaltsverzeichnis ▼
- Was ist Osmose in der Biologie?
- Wie funktioniert Osmose? (Schritt für Schritt)
- Hypo-, iso- und hypertonisch: Was ist der Unterschied?
- Osmose in Pflanzenzellen: Turgor und Plasmolyse
- Osmose in Tierzellen: Hämolyse und Krenation
- Was ist osmotischer Druck?
- Osmose vs. Diffusion: Was ist der Unterschied?
- Osmose-Beispiele im Alltag und in der Natur
- Schritt-für-Schritt Trainer
- Übungsaufgaben
- Karteikarten
- Video
- Zusammenfassung
Was ist Osmose in der Biologie?
Osmose ist die gerichtete Diffusion von Wasser durch eine semipermeable (halbdurchlässige) Membran – von der geringer konzentrierten Seite zur höher konzentrierten Seite. Einfacher gesagt: Wasser wandert immer dorthin, wo mehr gelöste Teilchen sind, um die Konzentration beiderseits der Membran auszugleichen.
Warum ist das so wichtig? Weil Osmose der Schlüsselmechanismus ist, über den Pflanzen Wasser aus dem Boden aufnehmen, durch den Blutzellen ihre Form behalten und durch den Nierenzellen den Wasserhaushalt des Körpers regulieren. Ohne Osmose gäbe es kein Leben, wie wir es kennen.
Der Begriff semipermeabel ist hier entscheidend: Die Membran lässt Wasser (das Lösungsmittel) durch, nicht aber die gelösten Teilchen wie Zucker oder Salzionen. Gerade weil die Teilchen nicht hindurchkommen, entsteht das Konzentrationsgefälle, das das Wasser antreibt.
Osmose läuft passiv ab – das heißt, die Zelle braucht dafür keine Energie (kein ATP). Das Wasser folgt allein dem Konzentrationsgefälle, ähnlich wie Wasser einen Berg hinunterfließt.
Osmose lernen?
Wie funktioniert Osmose? (Schritt für Schritt)
Stell dir vor, du trennst zwei Lösungen mit unterschiedlicher Zuckerkonzentration durch eine semipermeable Membran. Auf der einen Seite ist viel Zucker (Seite A), auf der anderen Seite wenig Zucker (Seite B). Die Membran lässt Wasser durch, aber keinen Zucker. Was passiert?
-
1
Konzentrationsgefälle erkennen: Seite A hat mehr gelöste Teilchen (Zucker), also weniger freie Wassermoleküle pro Volumen. Seite B hat weniger gelöste Teilchen – hier gibt es mehr freie Wassermoleküle.
-
2
Wasserfluss setzt ein: Wasser diffundiert durch die Membran von Seite B (höheres Wasserpotenzial) nach Seite A (niedrigeres Wasserpotenzial). Es folgt dem Wasserpotenzialgradienten – einem Konzept, das Konzentration und Druck vereint.
-
3
Volumenänderung: Seite A schwillt an (mehr Wasser), Seite B verliert Volumen. Der Flüssigkeitsspiegel auf Seite A steigt sichtbar.
-
4
Osmotisches Gleichgewicht: Der Wasserfluss stoppt, wenn der osmotische Druck (die Sogkraft durch Konzentrationsdifferenz) dem hydrostatischen Druck (Gewicht der Flüssigkeitssäule) entspricht. Ab diesem Punkt ist das System im Gleichgewicht.
In der Biologie spricht man oft vom Wasserpotenzial (griech. Psi, Ψ). Reines Wasser hat den Wert Ψ = 0. Gelöste Stoffe senken das Wasserpotenzial (negativere Werte). Wasser fließt immer von höherem (weniger negativ) zu niedrigerem Wasserpotenzial (negativer). Für den Schulunterricht genügt oft die Kurzregel: Wasser folgt den gelösten Teilchen.
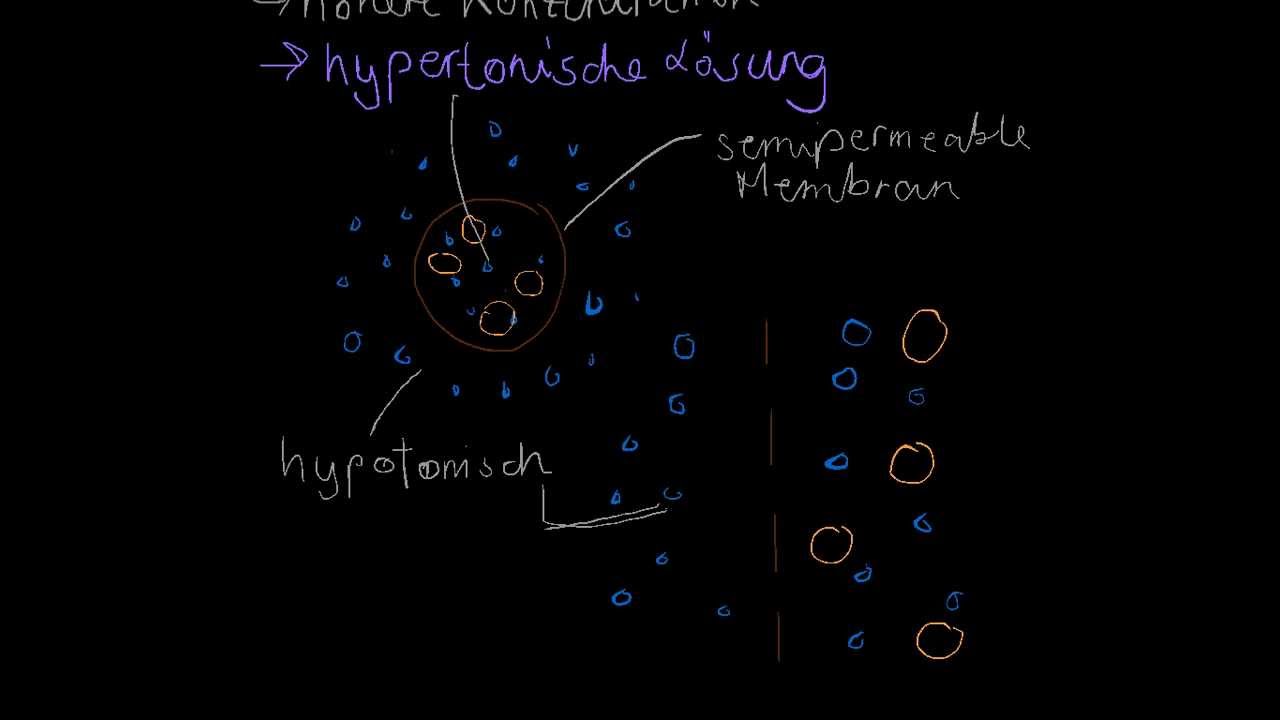
Hypo-, iso- und hypertonisch: Was ist der Unterschied?
Je nachdem, wie konzentriert die Umgebungslösung im Vergleich zum Zellinneren ist, verhalten sich Zellen ganz unterschiedlich. Biologie unterscheidet drei Fälle – und die Fachbegriffe dazu sind Pflichtlernstoff:
| Begriff | Konzentration außen | Wasserfluss | Effekt auf Zelle |
|---|---|---|---|
| Hypotonisch | Geringer als innen | Wasser strömt ein | Zelle schwillt an (Turgeszenz) |
| Isotonisch | Gleich wie innen | Kein Nettofluss | Zelle bleibt gleich |
| Hypertonisch | Höher als innen | Wasser strömt aus | Zelle schrumpft (Plasmolyse) |
Viele Schüler*innen vergessen: Die Begriffe beziehen sich immer auf die Außenlösung im Vergleich zum Zellinneren. Eine hypertonische Lösung außen bedeutet: außen konzentrierter als innen – Wasser verlässt die Zelle.
Ein praktisches Beispiel zum Einprägen: Kochsalzlösung mit 0,9 % NaCl ist isotonisch zum menschlichen Blut – deswegen wird genau diese Konzentration als physiologische Kochsalzlösung in der Medizin verwendet. Bei Infusionen verhindert man so, dass rote Blutkörperchen schrumpfen oder platzen.
Was ist Turgor und wie entsteht Plasmolyse in Pflanzenzellen?
Pflanzenzellen haben zusätzlich zur Zellmembran eine starre Zellwand – das ändert das Bild der Osmose erheblich. Wenn Wasser in eine Pflanzenzelle strömt, drückt der Zellinhalt gegen die Zellwand und erzeugt einen inneren Druck: den Turgordruck.
Turgor: der Stützdruck der Pflanzen
Turgordruck ist lebensnotwendig für Pflanzen. Er hält Blätter aufrecht, lässt Blüten ihre Form behalten und ermöglicht das Öffnen und Schließen der Spaltöffnungen (Stomata). Eine ausreichend bewässerte Pflanze ist prall und fest – das ist der Turgor. Trocknet die Pflanze aus, sinkt der Turgordruck und sie welkt.
Plasmolyse: wenn Zellen ihr Wasser verlieren
In hypertonischer Lösung verliert eine Pflanzenzelle durch Osmose so viel Wasser, dass sich der Protoplast (Zellinhalt + Membran) von der Zellwand löst. Dieser Vorgang heißt Plasmolyse. Die Zellwand bleibt stehen, der Protoplast zieht sich zurück – man sieht unter dem Mikroskop den entstehenden Spalt.
Wichtig: Plasmolyse ist in der Regel reversibel. Gibt man der Zelle wieder Wasser (hypotone Lösung), strömt Wasser zurück, der Protoplast schwillt an und legt sich wieder an die Zellwand – dieser Vorgang heißt Deplasmolyse.
Wie wirkt Osmose auf Tierzellen? Hämolyse und Krenation
Tierzellen – zum Beispiel rote Blutkörperchen – haben keine Zellwand. Daher können osmotische Kräfte die Zelle viel leichter verformen oder sogar zerstören.
Hypotonische Umgebung: Hämolyse
Wird eine Zelle in destilliertes Wasser (hypotonische Umgebung) gelegt, strömt durch Osmose Wasser ins Zellinnere. Ohne schützende Zellwand kann die Zelle anschwellen, bis die Membran platzt. Dieses Platzen einer roten Blutzelle nennt man Hämolyse (griech. haima = Blut, lysis = Auflösung).
Hypertonische Umgebung: Krenation
In hypertonischer Lösung verlässt Wasser die Zelle. Die rote Blutzelle schrumpft und bekommt einen gezackten, unregelmäßigen Rand – diesen Zustand nennt man Krenation. Die Zelle kann so ihre Funktion (Sauerstofftransport) nicht mehr erfüllen.
| Umgebung | Pflanzenzelle | Tierzelle (Erythrozyt) |
|---|---|---|
| Hypotonisch | Turgeszenz (Zellwand hält stand) | Hämolyse (Membran platzt) |
| Isotonisch | Grenzplasmolyse / Normal | Normal (physiologische Form) |
| Hypertonisch | Plasmolyse (Protoplast löst sich ab) | Krenation (Zelle schrumpft) |
Der entscheidende Unterschied zwischen Pflanzen- und Tierzellen bei der Osmose ist die Zellwand: Sie schützt Pflanzenzellen vor dem Platzen, ermöglicht Turgordruck und lässt Plasmolyse entstehen. Tierzellen fehlt dieser Schutz – hypotonische Umgebungen können sie direkt zerstören.
Was ist osmotischer Druck und wie berechnet man ihn?
Der osmotische Druck (Symbol: Π, griech. Pi) ist die Kraft, die nötig wäre, um den Wasserfluss durch eine semipermeable Membran zu stoppen. Je mehr gelöste Teilchen in einer Lösung, desto höher ihr osmotischer Druck – und desto stärker ist die "Sogwirkung" auf Wasser.
Die Formel \(\Pi = cRT\) gilt näherungsweise für verdünnte Lösungen:
- Π = osmotischer Druck (in Pa oder bar)
- c = molare Konzentration der gelösten Teilchen (in mol/L)
- R = allgemeine Gaskonstante (8,314 J·mol⁻¹·K⁻¹)
- T = absolute Temperatur (in Kelvin; K = °C + 273)
Beispielrechnung: Osmotischer Druck einer Salzlösung
Gegeben: Kochsalzlösung (NaCl), c = 0,15 mol/L (Natriumionen), T = 37 °C = 310 K
- 1
Konzentration: NaCl dissoziiert vollständig: c(gesamt) = 2 × 0,15 mol/L = 0,30 mol/L (Na⁺ und Cl⁻ getrennt)
- 2
Einsetzen: \(\Pi = 0{,}30 \cdot 8{,}314 \cdot 310 = 773\,\text{kPa} \approx 7{,}7\,\text{bar}\)
- 3
Vergleich: Das entspricht in etwa dem osmotischen Druck von Blutplasma (~7,8 bar) – kein Zufall, denn 0,9 % NaCl ist physiologische Kochsalzlösung.
In Krankenhäusern werden Infusionslösungen exakt auf isotonischen osmotischen Druck eingestellt (~285 mOsmol/kg). Zu viel oder zu wenig löst Hämolyse oder Krenation der Blutzellen aus. Das zeigt, wie lebenswichtig das genaue Verständnis von Osmose und osmotischem Druck ist.
Osmose vs. Diffusion: Was ist genau der Unterschied?
Osmose wird oft mit Diffusion verwechselt – beide sind passive Transportprozesse, aber es gibt einen entscheidenden Unterschied:
| Merkmal | Diffusion | Osmose |
|---|---|---|
| Was bewegt sich? | Gelöste Teilchen (Zucker, Ionen, Gase) | Lösungsmittel (meist Wasser) |
| Membrantyp nötig? | Nicht notwendig | Semipermeable Membran erforderlich |
| Richtung | Hoch → niedrige Konzentration (gelöste Stoffe) | Niedrig → hohe Konzentration (gelöste Stoffe) = Wasser folgt den Teilchen |
| Energiebedarf | Passiv (keine Energie) | Passiv (keine Energie) |
| Beispiel | Tinte löst sich im Wasser auf | Wasseraufnahme durch Pflanzenwurzeln |
Kurz gesagt: Osmose ist ein Spezialfall der Diffusion – nämlich die Diffusion des Lösungsmittels durch eine semipermeable Membran. Bei der normalen Diffusion diffundieren die gelösten Teilchen selbst.
Welche Osmose-Beispiele gibt es im Alltag und in der Natur?
Osmose ist kein abstraktes Laborkonzept – sie findet in jedem lebenden Organismus statt und erklärt viele alltägliche Phänomene:
Kirschen platzen im Regen
Reife Kirschen enthalten süßen Zellsaft mit hoher Zuckerkonzentration. Wenn Regenwasser (hypotonisch) auf die Kirschenhaut trifft, strömt Wasser durch die semipermeable Hautmembran ins Innere. Der Druck steigt, bis die Frucht platzt – eine klassische osmotische Hämolyse auf Fruchtebene.
Gurken in Salzlake: Konservierung durch Osmose
Saure Gurken werden in hochprozentige Salzlösung (hypertonisch) eingelegt. Wasser strömt aus den Gurkenzellen heraus, die Zellen schrumpfen und werden weicher. Die Pflanzenzellwände bleiben intakt – die Gurke wird knackig weich, und die Salzlake hemmt durch die niedrige Wasseraktivität das Bakterienwachstum. Dasselbe Prinzip nutzt man beim Einsalzen von Fleisch oder Käse.
Wasseraufnahme durch Pflanzenwurzeln
Pflanzenwurzelzellen enthalten gelöste Mineralsalze in höherer Konzentration als das Bodenwasser. Wasser strömt durch Osmose in die Wurzelzellen, wird durch den Turgordruck weitergeleitet und gelangt schließlich bis in die Blätter. Ohne Osmose gäbe es kein Pflanzenwachstum – und keine Landpflanzen.
Runzlige Haut beim Baden
Beim langen Baden in Leitungswasser (schwach hypotonisch) nimmt die oberste Hautschicht (Stratum corneum) durch Osmose Wasser auf und quillt auf – das erzeugt die typischen Falten. Finger und Zehen runzeln sich, Gesichtshaut eher nicht, weil die Schichten unterschiedlich dick sind.
Osmoregulation: Wie Organismen ihren Wasserhaushalt kontrollieren
Meerestiere wie Knochenfische trinken ständig Meerwasser und scheiden konzentrierten Harn aus, weil das Meerwasser hypertonisch zu ihrem Blut ist. Süßwasserfische haben das entgegengesetzte Problem – sie nehmen ständig Wasser auf und müssen verdünnten Harn produzieren. Der menschliche Körper reguliert den osmotischen Druck des Blutes durch die Nieren auf ca. 285–310 mOsmol/kg – abweichungen davon sind medizinische Notfälle.
Schritt-für-Schritt Trainer
Geh die folgenden Experimente schrittweise durch – klicke dich durch jeden Schritt, bevor du die Lösung siehst.
Übungsaufgaben zu Osmose
Teste dein Wissen mit diesen Aufgaben – von einfach bis anspruchsvoll.
Eine semipermeable (halbdurchlässige) Membran lässt bestimmte Teilchen durch, andere nicht. Bei der Osmose lässt sie das Lösungsmittel Wasser durch, aber keine gelösten Stoffe wie Zucker oder Salze. Genau dadurch entsteht das Konzentrationsgefälle, das den Wasserfluss antreibt.
Das Salz erzeugt eine hypertonische Lösung auf der Salatoberfläche. Das bedeutet: Die Konzentration der gelösten Teilchen außen (im Salz) ist höher als im Zellinneren. Wasser strömt durch Osmose aus den Salatblattzellen heraus. Die Zellen verlieren ihren Turgordruck, das Blatt wird weich und welk – und der Wasserfilm auf dem Salat zeigt das ausgetretene Zellwasser.
Pflanzenzelle: Wasser strömt durch Osmose ins Innere (hypotone Umgebung). Der Turgordruck steigt – die Zellwand verhindert jedoch ein Platzen. Die Zelle wird prall turgeszent. Erythrozyt (rote Blutzelle): Wasser strömt ebenfalls ins Innere. Da keine Zellwand vorhanden ist, schwillt die Zelle so stark an, bis die Membran platzt – das ist die Hämolyse. Entscheidend ist also das Vorhandensein einer Zellwand.
Gegeben: c = 0,2 mol/L = 200 mol/m³; T = 25 °C + 273 = 298 K; R = 8,314 J/(mol·K)
Berechnung: Π = c · R · T = 200 mol/m³ × 8,314 J/(mol·K) × 298 K ≈ 495.514 Pa ≈ 4,96 bar
Glucose dissoziiert nicht (Nichtionisierend), daher wird die Konzentration nicht multipliziert. Das Ergebnis von ~5 bar zeigt, wie erheblich der osmotische Druck selbst bei einer relativ verdünnten Lösung ist.
Meerwasserfische haben eine osmotische Konzentration im Blut (~350 mOsmol/kg), die geringer ist als die des Meerwassers (~1100 mOsmol/kg). Das Meerwasser ist also hypertonisch – Wasser strömt durch Osmose ständig aus dem Fisch heraus. Um das auszugleichen, trinken Meerwasserfische große Mengen Salzwasser und scheiden aktiv Salze über die Kiemen aus.
In Süßwasser wäre das umgekehrt: Das Süßwasser ist extrem hypotonisch. Der Fisch würde unkontrolliert Wasser aufnehmen, die Körperzellen würden anschwellen – ein tödliches osmotisches Ungleichgewicht. Meerwasserfische sind physiologisch nicht in der Lage, so viel Wasser über die Nieren auszuscheiden.
Karteikarten zum Einprägen
Klicke auf die Karte zum Umdrehen – navigiere mit den Pfeilen.
Erklärvideo zu Osmose und Diffusion
Schau dir das Video an, um Osmose und Diffusion noch einmal visuell zu erleben.
Zusammenfassung: Osmose in der Biologie
Die wichtigsten Punkte auf einen Blick
- Osmose = gerichteter Wasserfluss durch eine semipermeable Membran von niedrigerer zu höherer Konzentration (gelöste Teilchen)
- Semipermeable Membran: lässt Wasser durch, nicht aber gelöste Teilchen
- Hypotonisch = außen weniger konzentriert → Wasser strömt in die Zelle; Isotonisch = Gleichgewicht; Hypertonisch = außen konzentrierter → Wasser verlässt die Zelle
- Pflanzenzellen: Turgor (Innendruck durch Wasser in Vakuole) und Plasmolyse (Ablösung des Protoplasten bei Wasserverlust)
- Tierzellen ohne Zellwand: Hämolyse (Platzen in hypotonischer Lösung) oder Krenation (Schrumpfen in hypertonischer Lösung)
- Osmotischer Druck: Π = cRT – proportional zur Konzentration und Temperatur
- Osmose läuft passiv ab – kein Energieaufwand nötig
- Anwendungen: Osmoregulation (Niere), Konservierung, Medizin (physiologische Kochsalzlösung, 0,9 % NaCl)